Ответы
Лучшие творческие работы участников 2 тура проекта
- 7-8 класс: 12x16, 12x36, 12x151, 12x163, 12x225, 12x231, 12x287, 12x336, 12x359, 12x385, 12x442, 12x466, 12x549, 12x833, 12x897, 12x916, 12x954, 12x984, 12x988, 12x1091
- 9 класс: 12x10, 12x57, 12x66, 12x407, 12x436, 12x468, 12x689, 12x723, 112x840, 12x913, 12x970, 12x1025
- 10 класс: 12x31, 12x290, 12x293, 12x365, 12x373, 12x441, 12x1033
- 11 класс: 12x87, 12x121, 12x288, 12x387, 12x460, 12x471, 12x562, 12x565
Перейти на вопросы для 9 классов
Перейти на вопросы для 10 классов, решение расчетной задачи
Перейти на вопросы для 11 классов, решение расчетной задачи
Номинация 7-8 классы
Задание 1
Вещество, молекула которого состоит из четырех атомов, – это:
- сероводород
- тетрахлорид углерода
- аммиак
- вода
Правильный ответ: 3) аммиак.
Задание 2
Сумма коэффициентов в уравнении, представленном схемой: Н2О + Р2О5 = Н4Р2О7
равна:
- 2
- 4
- 3
- 6
Правильный ответ: 2) 4.
Задание 3
Химический процесс (в отличие от физических) – это:
- ржавление железа в воде
- плавление стали в конвертере
- плавление чугуна в домне
- сплавление железа с хромом
Правильный ответ: 1) ржавление железа в воде.
Задание 4
Массовая доля брома наибольшая в соединении:
- GaBr3
- AlBr3
- BBr3
- InBr3
Правильный ответ: 3) BBr3.
Задание 5
Масса (в граммах) 0,2 моль гидроксида калия равна:
- 11,2
- 14,8
- 28
- 280
Правильный ответ: 1) 11,2.
Задание 6
Количество вещества (моль) порции оксида натрия, содержащей 6,02·1023 атомов натрия, составит:
- 0,25
- 0,5
- 1
- 2
Правильный ответ: 2) 0,5.
Задание 7
Число электронов на внешнем энергетическом уровне одинаково для:
- атомов хлора, марганца, брома
- атомов калия, кальция, скандия
- частиц S2-; Ar; Br-;
Правильный ответ: 3) частиц S2-; Ar; Br-.
Задание 8
Укажите ряд элементов, которые в соединениях проявляют только степень окисления +1:
- Li, Na, H
- Li, Na, Cl
- Li, Rb, Cs
Правильный ответ: 3) Li, Rb, Cs.
Задание 9
Максимальная степень окисления брома в соединениях равна:
- -1
- -7
- +3
- +7
- +5.
Правильный ответ: 4) +7.
Задание 10
Два химических элемента имеют названия, в переводе с греческого означающие зеленый и фиолетовый. Назовите эти элементы.
Правильный ответ: хлор, йод.
Номинация 9 класс
Задание 1
Элементом, который проявляет в соединениях единственную степень окисления, является:
- водород
- кислород
- фтор
- медь
Правильный ответ: 3) фтор.
Задание 2
Молярная масса газа, 0,3 г которого занимает объем 0,224 л (н.у.), равна:
- 30 г/моль;
- 22,4 г/моль;
- 60 г/моль
Правильный ответ: 1) 30 г/моль.
Задание 3
Формулой оксида хрома, в состав которого входит 2,167 массовых частей хрома и 1,000 массовая часть кислорода, является:
- Cr2O3
- CrO
- CrO3
Правильный ответ: 1) Cr2O3. Посмотреть решение.
Задание 4
Массы водорода и кислорода, содержащихся в воде массой 1 кг, равны соответственно:
- 0,5 кг и 0,5 кг
- 0,11 кг и 0,89 кг
- 0,89 кг и 0,11 кг
- 0,34 кг и 0,66 кг
Правильный ответ: 2) 0,11 кг и 0,89 кг. Посмотреть решение.
Задание 5
Объем хлороводорода (н.у.), который потребуется для приготовления 1 л водного раствора, в котором массовая доля хлороводорода равна 0,12 (или 12%), а плотность равна 1,059 г/см3, равен:
- 12 л
- 78 л
- 22,4 л
- 87 л
Правильный ответ: 2) 78 л. Посмотреть решение.
Задание 6
Чему равна степень окисления и валентность атома азота в молекуле азотной кислоты?
- степень окисления +5; валентность IV
- степень окисления +5; валентность V
- степень окисления +4; валентность V
Правильный ответ: 1) степень окисления +5; валентность IV.
Задание 7
Только восстановителем в химических реакциях является:
- водород
- кремний
- медь
- графит
Правильный ответ: 3) медь.
Задание 8
При диссоциации 1 моля алюмокалиевых квасцов образуется катионов:
- 1 моль
- 2 моль
- 3 моль
- 4 моль
Правильный ответ: 2) 2 моль.
Задание 9
Сумма коэффициентов в уравнении окислительно-восстановительной реакции KClO3 + P → … равна:
- 18
- 15
- 21
- 19
Правильный ответ: 4) 19.
Задание 10
Самым тугоплавким металлом является:
- вольфрам
- титан
- лантан
- цирконий
Правильный ответ: 1) вольфрам.
Номинация 10 класс
Задание 1
Формула высшего оксида элемента с электронной конфигурацией 1s22s22p63s23p2
- Э2О
- ЭО2
- ЭО3
- ЭО
Правильный ответ: 2) ЭО2.
Задание 2
Реакция среды нейтральная в растворе соли:
- Rb2S
- Rb2CO3
- Rb2SO3
- Rb2SO4
Правильный ответ: 4) Rb2SO4.
Задание 3
К 400 г 18%-го раствора гидроксида калия добавили 100 г раствора, содержащего 0,5 моль того же вещества. Конечная массовая доля растворенного вещества (в процентах) равна:
- 20
- 25
- 30
- 40
Правильный ответ: 1) 20.
Задание 4
Диоксид серы реагирует с:
- CO2, O2
- KOH, KHCO3
- H2S, HCl
- H2SO4 (разб.); K2СO3
Правильный ответ: 2) KOH, KHCO3.
Задание 5
Смесь кальция и оксида кальция (массой каждого вещества по 15 г) обработали избытком разбавленной уксусной кислоты и собрали газ объемом … в литрах (н. у.).
- 2,1
- 4,2
- 8,4
- 16,8
Правильный ответ: 3) 8,4.
Задание 6
В реакции серебряного зеркала 0,66 г альдегида образует 3,24 г осадка. Молекулярная формула альдегида:
- CH3CHO
- HCHO
- C2H5CHO
- C3H7CHO
Правильный ответ: 1) CH3CHO.
Задание 7
В пробирке 1 находится бромная вода. В нее внесли палочку с прилипшими кристаллами неизвестного органического вещества. В пробирках с номерами 2-5 показаны происходящие изменения в течение нескольких секунд. Какие предположения о внесенном веществе (укажите его название) можно сделать, оценивая признаки проходящих реакций?

Правильный ответ: фенол.
Задание 8
Для осуществления схемы превращений подберите необходимые реагенты, дайте название углеводороду Х1. Ответ состоит из цифр – номеров реагентов. приведенных в последовательности указанных превращений первых двух стадий и названия соединения Х1. Пример оформления ответа: 1,2 (толуол).
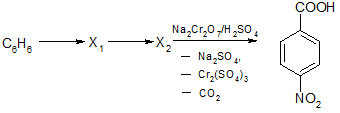
Реагенты:
- HNO3 + H2SO4
- CH3OH, H3PO4
- этилен, H3PO4
- пропен, H3PO4
Правильный ответ: 4,1 (изопропилбензол) и 3,1.
Комментарий научного руководителя: Уважаемые участники проекта, в задании №8 мы расширили ответ, добавив вариант "3,1", поскольку в условии задачи по техническим причинам исчезла цифра 2 перед СО2 и будут учитываться оба ответа в равной степени.
Задание 9
Дайте названия веществам (A, B, D, C, E), участвующим в приведенной схеме превращений:
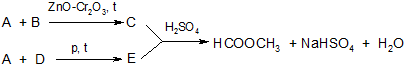
Правильный ответ:
А – оксид углерода (II) (угарный газ)
В – водород
D – гидроксид натрия
C – метиловый спирт (метанол)
E – формиат натрия (метаноат натрия)
Задание 10
Назовите элемент, в атоме которого на предвнешнем уровне находится 13 электронов, а на четвертом внешнем – 2 электрона:
- технеций;
- железо;
- марганец;
- кобальт.
Правильный ответ: 3) марганец.
Номинация 11 класс
Задание 1
Плотность по водороду газовой смеси из 56 л аргона (н.у.) и 28 л азота (н.у.) равна:
- 16
- 18
- 19,5
- 22
Правильный ответ: 2) 18.Посмотреть решение.
Задание 2
Выберите ряд веществ, в котором энергия химической связи уменьшается, а длина связи возрастает:
- СН4; SiH4; GeH4
- H2S; H2O; SeH2
- HBr; HJ; HCl
- AsH3; NH3; PH3
Правильный ответ: 1) СН4; SiH4; GeH4.
Задание 3
Вещество в твердом агрегатном состоянии характеризуется низкой температурой плавления и кипения, высокой летучестью. Следовательно, кристаллическая решетка вещества:
- атомная
- ионная
- металлическая
- молекулярная
Правильный ответ: 4) молекулярная.
Задание 4
В ряду веществ: НF; HCl; HBr; HJ энергия межмолекулярных водородных связей:
- увеличивается
- уменьшается
- не изменяется
- увеличивается, а затем уменьшается.
Правильный ответ: 2) уменьшается.
Задание 5
Полярность химической связи наибольшая в частице:
- СО
- ВF3
- NF3
- NO
Правильный ответ: 2) ВF3.
Задание 6
В пробирках 1 и 2 находятся водные растворы этилового спирта и фенола. В растворы опускают одинаковые стеклянные палочки с нанесенным на конец палочки неизвестным веществом.
Помешивая палочкой в растворах, наблюдают за происходящими внешними изменениями окраски растворов, которые можно заметить на этих стоп-кадрах (7 состояний).
Затем одну из пробирок помещают в пламя спиртовки и осторожно, при встряхивании раствора нагревают в течение минуты.
Какое вещество внесено в пробирки с растворами? В какой пробирке находится раствор этилового спирта, а в какой – раствор фенола (установите соответствие).

Правильный ответ:
Внесенное вещество – перманганат калия
1 пробирка – фенол
2 пробирка – этиловый спирт
Задание 7
Навеску 26,8 г смеси двух одноосновных органических кислот растворили в воде. Половину раствора обработали избытком аммиачного раствора оксида серебра, при этом выделилось 21,6 г серебра. На нейтрализацию другой половины раствора потребовалось 0,2 моль гидроксида натрия. Определите: какие кислоты растворены в воде и какова масса каждой из кислот в смеси (в граммах). Ответом служат названия кислот и их масса, пример ответа: пропановая кислота (0,1 г); пентановая кислота (21.1 г)
Правильный ответ:
метановая кислота (9,2 г);
бутановая кислота (17,6 г).
Задание 8
При полном сгорании навески газообразного углеводорода, широко применяющегося в промышленном органическом синтезе, масса образовавшейся воды оказалась равной массе исходной навески. Определите строение углеводорода. Ответом служит название углеводорода (IUPAC).
Правильный ответ: бутадиен-1,3.
Задание 9
При нитровании бензола получен продукт, для полного восстановления 2,07 г которого необходим раствор 14,4 г нонагидрата сульфида натрия (в ходе восстановления выпадает желтоватый осадок). Определите вероятный качественный и количественный состав продукта нитрования. Условия реакции нитрования не приводятся.
Правильный ответ: нитробензол (0,015 моль); динитробензол (0,005 моль).
Задание 10
Установите структурную формулу соединения С6Н12Cl2, если при гидролизе оно переходит в карбонильное соединение, а при окислении последнего образуется смесь ацетона, уксусной, пропионовой и 2-метилпропионовой кислот. Ответом служит название вещества (IUPAC) .
Правильный ответ: 2-метил-3,3-дихлорпентан.
Возникли вопросы?
- Электронная почта (e-mail): chemproject@edu.yar.ru
- Телефон: +7 (4852) 32-88-91, 30-29-62
- Конференц-связь MS Lync: aliya@unicom.edu.yar.ru (для участников из Ярославской области)